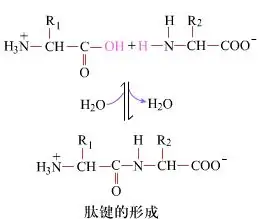
Op die oppervlak is die vorming van peptiedbindings, wat dipeptiede lewer, 'n eenvoudige chemiese proses.Dit beteken dat die twee aminosuurkomponente deur 'n peptiedbinding, 'n amiedbinding, verbind word terwyl dit gedehidreer word.
Peptiedbindingsvorming is die aktivering van 'n aminosuur onder ligte reaksietoestande.(A) karboksieleenheid, tweede aminosuur (B) Die nukleofiele geaktiveerde karboksieleenheid vorm dan die dipeptied (AB)."As die karboksielkomponent (A) nie beskerm word nie, kan die vorming van die peptiedbinding nie beheer word nie."Byprodukte soos lineêre en sikliese peptiede kan met teikenverbindings AB gemeng word.Daarom moet alle funksionele groepe wat nie by peptiedbindingsvorming betrokke is nie, op 'n tydelike omkeerbare wyse tydens peptiedsintese beskerm word.
Dus, peptiedsintese - die vorming van elke peptiedbinding - behels drie stappe van aggregasie.
Die eerste stap is om 'n paar aminosure voor te berei wat beskerming benodig, en die zwitterioniese struktuur van aminosure bestaan nie meer nie.
Die tweede stap is 'n tweestap-reaksie om peptiedbindings te vorm, waarin die karboksielgroep van die N-beskermde aminosuur eers na die aktiewe tussenproduk geaktiveer word en dan word die peptiedbinding gevorm.Hierdie gekoppelde reaksie kan óf as 'n eenstap-reaksie óf as twee opeenvolgende reaksies plaasvind.
Die derde stap is die selektiewe verwydering of volledige verwydering van die beskermende basis.Alhoewel alle verwydering eers kan plaasvind nadat alle peptiedkettings saamgestel is, is selektiewe verwydering van beskermende groepe ook nodig om die peptiedsintese voort te sit.
Omdat 10 aminosure (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec en Cys) syketting funksionele groepe bevat, wat selektiewe beskerming vereis, wat peptiedsintese meer ingewikkeld maak.Tydelike en semi-permanente beskermingsbasisse moet onderskei word vanweë die verskillende vereistes vir selektiwiteit.Tydelike beskermingsgroepe word in die volgende stap gebruik om die tydelike beskerming van aminosuur- of karboksielfunksionele groepe te weerspieël.Semi-permanente beskermende groepe word verwyder sonder om in te meng met reeds gevormde peptiedbindings of aminosuur-sykettings, soms tydens sintese.
"Ideaal gesproke moet aktivering van die karboksielkomponent en die daaropvolgende vorming van peptiedbindings (koppelingsreaksies) vinnig wees, sonder rasemiese of neweprodukvorming, en molêre reaktante moet toegepas word om hoë opbrengste te behaal."Ongelukkig voldoen nie een van die chemiese koppelingsmetodes aan hierdie vereistes nie, en min is geskik vir praktiese sintese.
Tydens peptiedsintese word die funksionele groepe wat by verskeie reaksies betrokke is gewoonlik aan die handsentrum gekoppel, glisien is die enigste uitsondering, en daar is 'n potensiële risiko van rotasie.
Die laaste stap in die peptiedsintese-siklus is die verwydering van alle beskermende groepe.Selektiewe verwydering van beskermende groepe is belangrik vir peptiedkettingverlenging bykomend tot die vereiste vir volledige verwydering van beskerming in dipeptiedsintese.Sintetiese strategieë moet noukeurig beplan word.Na gelang van die strategiese keuse, kan N die α-amino- of karboksielbeskermende groepe selektief verwyder.Die term "strategie" verwys na die volgorde van kondensasiereaksies van individuele aminosure.Oor die algemeen is daar 'n verskil tussen geleidelike sintese en fragmentkondensasie.Peptiedsintese (ook bekend as "konvensionele sintese") vind in oplossing plaas.In die meeste gevalle kan geleidelike verlenging van die peptiedketting slegs gesintetiseer word deur die peptiedketting te gebruik om korter fragmente te sintetiseer.Om langer peptiede te sintetiseer, moet die teikenmolekules in gepaste fragmente gesegmenteer word en bepaal word dat hulle die mate van differensiasie by die C-terminus kan minimaliseer.Nadat die individuele fragmente geleidelik saamgevoeg is, sal die teikenverbinding saamgevoeg word.Die strategie van peptiedsintese sluit die keuse van die beste en mees geskikte beskermende fragment in, en die strategie van peptiedsintese sluit die keuse van die mees geskikte kombinasie van beskermende basisse en die beste metode van fragmentvervoeging in.
Postyd: 19 Julie 2023