Peptiede is 'n klas verbindings wat gevorm word deur die verbinding van veelvuldige aminosure deur peptiedbindings.Hulle is alomteenwoordig in lewende organismes.Tot dusver is tienduisende peptiede in lewende organismes gevind.Peptiede speel 'n belangrike rol in die regulering van die funksionele aktiwiteite van verskeie stelsels, organe, weefsels en selle en in lewensaktiwiteite, en word dikwels gebruik in funksionele analise, teenliggaamnavorsing, geneesmiddelontwikkeling en ander velde.Met die ontwikkeling van biotegnologie en peptiedsintese-tegnologie, is meer en meer peptiedmiddels ontwikkel en in die kliniek toegepas.
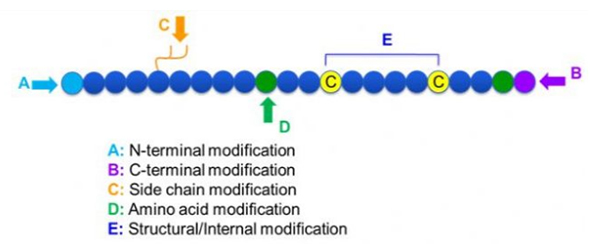
Daar is 'n wye verskeidenheid peptiedmodifikasies, wat eenvoudig verdeel kan word in postmodifikasie en prosesmodifikasie (met gebruik van afgeleide aminosuurmodifikasie), en N-terminale modifikasie, C-terminale modifikasie, sykettingmodifikasie, aminosuurmodifikasie, skeletmodifikasie, ens., afhangende van die wysigingswerf (Figuur 1).As 'n belangrike manier om die hoofkettingstruktuur of sykettinggroepe van peptiedkettings te verander, kan peptiedmodifikasie die fisiese en chemiese eienskappe van peptiedverbindings effektief verander, wateroplosbaarheid verhoog, die aksietyd in vivo verleng, hul biologiese verspreiding verander, immunogenisiteit uitskakel , verminder toksiese newe-effekte, ens. In hierdie vraestel word verskeie belangrike peptiedmodifikasiestrategieë en hul kenmerke bekendgestel.
1. Siklisering
Sikliese peptiede het baie toepassings in biogeneeskunde, en baie natuurlike peptiede met biologiese aktiwiteit is sikliese peptiede.Omdat sikliese peptiede geneig is om meer rigied as lineêre peptiede te wees, is hulle uiters bestand teen die spysverteringstelsel, kan hulle in die spysverteringskanaal oorleef en toon 'n sterker affiniteit vir teikenreseptore.Siklisering is die mees direkte manier om sikliese peptiede te sintetiseer, veral vir peptiede met 'n groot strukturele skelet.Volgens die sikliseringsmodus kan dit verdeel word in syketting-kantkettingtipe, terminaal - sykettingtipe, terminaal - terminaaltipe (eind-tot-eindtipe).
(1) syketting-tot-syketting
Die mees algemene tipe syketting tot syketting siklisering is disulfiedoorbrugging tussen sisteïenreste.Hierdie siklisering word ingebring deur 'n paar sisteïenreste wat ontskerm word en dan geoksideer word om disulfiedbindings te vorm.Polisikliese sintese kan bereik word deur selektiewe verwydering van sulfhidrielbeskermingsgroepe.Siklisering kan óf in 'n post-dissosiasie oplosmiddel of op 'n pre-dissosiasie hars gedoen word.Siklisering op harse kan minder effektief wees as oplosmiddel siklisering omdat die peptiede op harse nie geredelik siklifiseerde konformasies vorm nie.Nog 'n tipe syketting-syketting siklisering is die vorming van 'n amiedstruktuur tussen 'n asparaginsuur- of glutamiensuurresidu en die basisaminosuur, wat vereis dat die sykettingbeskermingsgroep selektief van die polipeptied verwyder moet word. op die hars of na dissosiasie.Die derde tipe syketting-syketting siklisering is die vorming van difeniel-eters deur tirosien of p-hidroksifenielglisien.Hierdie tipe siklisering in natuurlike produkte word slegs in mikrobiese produkte aangetref, en sikliseringsprodukte het dikwels potensiële medisinale waarde.Die voorbereiding van hierdie verbindings vereis unieke reaksietoestande, dus word hulle nie dikwels in die sintese van konvensionele peptiede gebruik nie.
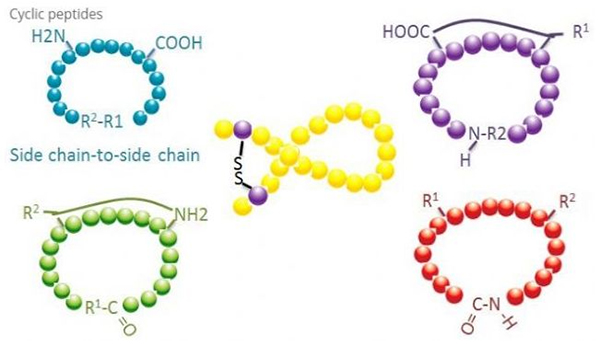
(2) terminaal-tot-syketting
Terminale-syketting siklisering behels gewoonlik die C-terminaal met die aminogroep van die lisien- of ornitien-syketting, of die N-terminaal met die asparaginsuur- of glutamiensuur-syketting.Ander polipeptied-siklisasie word gemaak deur eterbindings tussen terminale C en serien- of treonien-sykettings te vorm.
(3) Terminale of kop-tot-stert tipe
Kettingpolipeptiede kan óf in 'n oplosmiddel gesirkel word óf op 'n hars gefixeer word deur sykettingsiklus.Lae konsentrasies peptiede moet in oplosmiddelsentralisasie gebruik word om oligomerisering van peptiede te vermy.Die opbrengs van 'n kop-tot-stert sintetiese ring polipeptied hang af van die volgorde van die ketting polipeptied.Daarom, voordat sikliese peptiede op 'n groot skaal voorberei word, moet 'n biblioteek van moontlike gekettingde loodpeptiede eers geskep word, gevolg deur siklisering om die volgorde met die beste resultate te vind.
2. N-metilering
N-metilering kom oorspronklik voor in natuurlike peptiede en word in peptiedsintese ingebring om die vorming van waterstofbindings te voorkom, waardeur peptiede meer bestand teen biodegradasie en opruiming maak.Sintese van peptiede met behulp van N-gemetileerde aminosuurderivate is die belangrikste metode.Daarbenewens kan Mitsunobu-reaksie van N-(2-nitrobenseensulfonielchloried) polipeptied-hars tussenprodukte met metanol ook gebruik word.Hierdie metode is gebruik om sikliese peptiedbiblioteke wat N-gemetileerde aminosure bevat, voor te berei.
3. Fosforilering
Fosforilering is een van die mees algemene post-translasionele modifikasies in die natuur.In menslike selle is meer as 30% van proteïene gefosforileer.Fosforilering, veral omkeerbare fosforilering, speel 'n belangrike rol in die beheer van baie sellulêre prosesse, soos seintransduksie, geenuitdrukking, selsiklus en sitoskeletregulering, en apoptose.
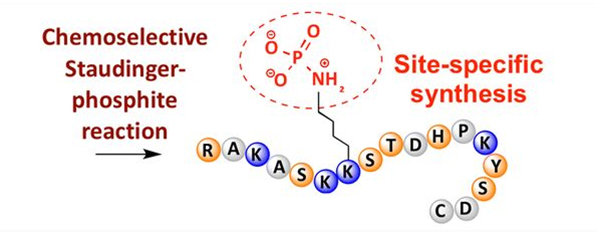
Fosforilering kan waargeneem word by 'n verskeidenheid van aminosuurreste, maar die mees algemene fosforilering teikens is serien, treonien, en tirosien residue.Fosfotirosien-, fosfotreonien- en fosfoserienderivate kan óf tydens sintese in peptiede ingebring word óf na peptiedsintese gevorm word.Selektiewe fosforilering kan bereik word deur gebruik te maak van residue van serien, treonien en tirosien wat beskermende groepe selektief verwyder.Sommige fosforileringsreagense kan ook fosforsuurgroepe in die polipeptied inbring deur postmodifikasie.In onlangse jare is plekspesifieke fosforilering van lisien bereik met behulp van 'n chemies selektiewe Staudinger-fosfietreaksie (Figuur 3).
4. Myristoilering en palmitoilering
Asylering van die N-terminaal met vetsure laat peptiede of proteïene toe om aan selmembrane te bind.Die gemyridamoyleerde volgorde op die N-terminaal stel Src familie proteïenkinases en omgekeerde transkriptase Gaq proteïene in staat om geteiken te word om aan selmembrane te bind.Myristiensuur is gekoppel aan die N-terminaal van die hars-polipeptied deur gebruik te maak van standaard koppelingsreaksies, en die resulterende lipopeptied kon onder standaard toestande gedissosieer en deur RP-HPLC gesuiwer word.
5. Glikosilering
Glikopeptiede soos vankomisien en teikolanien is belangrike antibiotika vir die behandeling van dwelm-weerstandige bakteriële infeksies, en ander glikopeptiede word dikwels gebruik om die immuunstelsel te stimuleer.Daarbenewens, aangesien baie mikrobiese antigene geglikosileer is, is dit van groot belang om glikopeptiede te bestudeer om die terapeutiese effek van infeksie te verbeter.Aan die ander kant is daar gevind dat die proteïene op die selmembraan van tumorselle abnormale glikosilering vertoon, wat maak dat glikopeptiede 'n belangrike rol speel in kanker- en tumor-immuunverdedigingsnavorsing.Glikopeptiede word berei deur Fmoc/t-Bu metode.Geglikosileerde oorblyfsels, soos treonien en serien, word dikwels in polipeptiede ingebring deur pentafluorofenolester-geaktiveerde fMOC's om geglikosileerde aminosure te beskerm.
6. Isopreen
Isopentadienilering vind plaas op sisteïenreste in die syketting naby die C-terminaal.Proteïen isopreen kan selmembraanaffiniteit verbeter en proteïen-proteïen interaksie vorm.Isopentadieneerde proteïene sluit in tyrosienfosfatase, klein GTase, cochaperone molekules, kern lamina en sentromere bindende proteïene.Isopreen polipeptiede kan voorberei word deur isopreen op harse te gebruik of deur sisteïenderivate in te voer.
7. Poliëtileenglikol (PEG) modifikasie
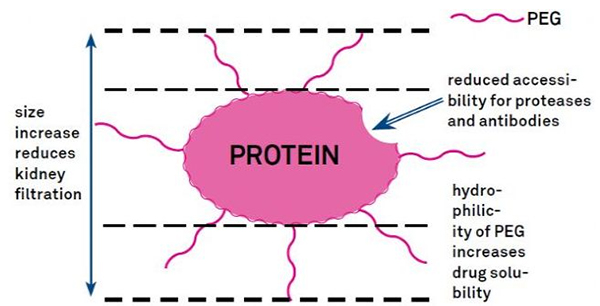
PEG-modifikasie kan gebruik word om proteïenhidrolitiese stabiliteit, bioverspreiding en peptiedoplosbaarheid te verbeter.Die bekendstelling van PEG-kettings aan peptiede kan hul farmakologiese eienskappe verbeter en ook die hidrolise van peptiede deur proteolitiese ensieme inhibeer.PEG-peptiede gaan makliker deur die glomerulêre kapillêre dwarssnit as gewone peptiede, wat die renale opruiming aansienlik verminder.As gevolg van die verlengde aktiewe halfleeftyd van PEG-peptiede in vivo, kan die normale behandelingsvlak gehandhaaf word met laer dosisse en minder gereelde peptiedmiddels.PEG-modifikasie het egter ook negatiewe effekte.Groot hoeveelhede PEG verhoed dat die ensiem die peptied afbreek en verminder ook die peptied se binding aan die teikenreseptor.Maar PEG-peptiede se lae affiniteit word gewoonlik geneutraliseer deur hul langer farmakokinetiese halfleeftyd, en deur langer in die liggaam teenwoordig te wees, het PEG-peptiede 'n groter waarskynlikheid om in teikenweefsels opgeneem te word.Daarom moet PEG-polimeerspesifikasies geoptimaliseer word vir optimale resultate.Aan die ander kant akkumuleer PEG-peptiede in die lewer as gevolg van verminderde renale opruiming, wat lei tot makromolekulêre sindroom.Daarom moet PEG-modifikasies versigtiger ontwerp word wanneer peptiede vir dwelmtoetsing gebruik word.
Algemene modifikasiegroepe van PEG-modifiseerders kan rofweg soos volg opgesom word: Amino (-amien) -NH2, aminometiel-Ch2-NH2, hidroksie-OH, karboksie-Cooh, sulfhidriel (-Tiol) -SH, Maleimied -MAL, suksinimiedkarbonaat - SC, succinimied asetaat -SCM, succinimied propionaat -SPA, n-hidroksisuksinimied -NHS, Acrylate-ch2ch2cooh, aldehied -CHO (soos propional-ald, butyrALD), akrielbasis (-akrilaat-akrl), asido-asied, biotiniel Biotien, Fluoresien, glutariel -GA, Akrilaathidrasied, alkyn-alkyn, p-tolueensulfonaat -OTs, suksinimiedsuksinaat -SS, ens. PEG-derivate met karboksielsure kan aan n-terminale amiene of lisien-sykettings gekoppel word.Amino-geaktiveerde PEG kan aan asparaginsuur- of glutamiensuur-sykettings gekoppel word.Mal-geaktiveerde PEG kan gekonjugeer word aan merkaptaan van ten volle ontskermde sisteïen-sykettings [11].PEG-modifiseerders word algemeen soos volg geklassifiseer (let wel: mPEG is metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) reguit ketting PEG wysiger
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunksionele PEG wysiger
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) vertakking PEG wysiger
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinisering
Biotien kan sterk met avidien of streptavidien gebind word, en die bindingssterkte is selfs naby aan kovalente binding.Biotien-gemerkte peptiede word algemeen gebruik in immunotoetsing, histositochemie en fluoressensie-gebaseerde vloeisitometrie.Gemerkte antibiotien-teenliggaampies kan ook gebruik word om gebiotinileerde peptiede te bind.Biotien-etikette word dikwels aan die lisiensyketting of die N-terminaal geheg.6-aminokapronsuur word dikwels gebruik as 'n binding tussen peptiede en biotien.Die binding is buigsaam in binding aan die substraat en bind beter in die teenwoordigheid van steriese hindering.
9. Fluorescerende etikettering
Fluorescerende etikettering kan gebruik word om polipptiede in lewende selle op te spoor en om ensieme en werkingsmeganismes te bestudeer.Triptofaan (Trp) is fluoresserend, dus kan dit vir intrinsieke etikettering gebruik word.Die emissiespektrum van triptofaan hang af van die perifere omgewing en neem af met dalende oplosmiddelpolariteit, 'n eienskap wat nuttig is vir die opsporing van peptiedstruktuur en reseptorbinding.Triptofaanfluoressensie kan geblus word deur geprotoneerde asparaginsuur en glutamiensuur, wat die gebruik daarvan kan beperk.Die Dansylchloriedgroep (Dansyl) is hoogs fluoresserend wanneer dit aan 'n aminogroep gebind word en word dikwels as 'n fluoresserende etiket vir aminosure of proteïene gebruik.
Fluoresensie-resonansie Energie-omskakeling (FRET) is nuttig vir ensiemstudies.Wanneer FRET toegedien word, bevat die substraat polipeptied gewoonlik 'n fluoressensie-etiketteringsgroep en 'n fluoressensie-blusgroep.Gemerkte fluoresserende groepe word geblus deur die uitblusmiddel deur nie-foton energie-oordrag.Wanneer die peptied van die betrokke ensiem gedissosieer word, straal die merkende groep fluoressensie uit.
10. Hok polipeptiede
Hokpeptiede het opties verwyderbare beskermende groepe wat die peptied beskerm teen binding aan die reseptor.Wanneer dit aan UV-straling blootgestel word, word die peptied geaktiveer, wat sy affiniteit met die reseptor herstel.Omdat hierdie optiese aktivering volgens tyd, amplitude of ligging beheer kan word, kan hokpeptiede gebruik word om reaksies wat in selle voorkom, te bestudeer.Die mees algemeen gebruikte beskermende groepe vir hokpolipeptiede is 2-nitrobensielgroepe en hul derivate, wat in peptiedsintese ingevoer kan word via beskermende aminosuurderivate.Aminosuurderivate wat ontwikkel is, is lisien, sisteïen, serien en tirosien.Aspartaat- en glutamaatderivate word egter nie algemeen gebruik nie as gevolg van hul vatbaarheid vir siklisering tydens peptiedsintese en -dissosiasie.
11. Poliantigeniese peptied (MAP)
Kort peptiede is gewoonlik nie immuun nie en moet aan draerproteïene gekoppel word om teenliggaampies te produseer.Poliantigeniese peptied (MAP) is saamgestel uit veelvuldige identiese peptiede wat aan lisienkerne gekoppel is, wat spesifiek hoë-sterkte-immunogene kan uitdruk en gebruik kan word om peptied-draer-proteïenkoeplette voor te berei.MAP-polipeptiede kan gesintetiseer word deur vastefase-sintese op MAP-hars.Onvolledige koppeling lei egter tot ontbrekende of afgekapte peptiedkettings op sommige takke en vertoon dus nie die eienskappe van die oorspronklike MAP polipeptied nie.As alternatief kan peptiede apart voorberei en gesuiwer word en dan aan MAP gekoppel word.Die peptiedvolgorde wat aan die peptiedkern geheg is, is goed gedefinieer en word maklik deur massaspektrometrie gekenmerk.
Afsluiting
Peptiedmodifikasie is 'n belangrike manier om peptiede te ontwerp.Chemies gemodifiseerde peptiede kan nie net hoë biologiese aktiwiteit handhaaf nie, maar ook effektief die nadele van immunogenisiteit en toksisiteit vermy.Terselfdertyd kan chemiese modifikasie peptiede met 'n paar nuwe uitstekende eienskappe gee.In onlangse jare is die metode van CH-aktivering vir die post-modifikasie van polipeptiede vinnig ontwikkel, en baie belangrike resultate is bereik.
Postyd: 20 Maart 2023
